Шестаев А.Ю., Протощак В.В., Гордеев В.В., Матич А.И., Гулько А.М.
Частота встречаемости доброкачественной гиперплазии предстательной железы (ДГПЖ) у лиц мужского пола в возрасте 50-60 лет составляет 40%, среди мужчин старше 90 лет этот показатель достигает 90% [1].
Инфравезикальная обструкция, возникающая вследствие развития ДГПЖ, приводит к снижению физиологической емкости мочевого пузыря, а также способствует развитию его гиперактивности. Среди всех симптомов нижних мочевых путей (СНМП) у больных ДГПЖ именно ноктурия в большей степени снижает качество жизни. Частое ночное мочеиспускание, как правило, становится причиной бессонницы, снижения дневной функциональной активности, а также повышения риска бытового травматизма [2,3].
Выделяют несколько этиологических факторов развития ноктурии: суточную полиурию, ночную полиурию, снижение ночной емкости мочевого пузыря, а также смешанный генез.
Особое внимание исследователей, занимающихся вопросами учащенного ночного мочеиспускания, уделяется поиску взаимосвязи ноктурии с расстройством сна. В настоящее время существует две точки зрения по данному вопросу. Первая – это «урологическая теория», которая указывает на то, что одной из главных причин инсомнии являются позывы к мочеиспусканию. Вторая точка зрения принадлежит специалистам, преимущественно занимающимися вопросами нарушения сна. Последние утверждают наоборот, что именно бессонница обусловливает ноктурию [4]. Также доказано, что нарушение суточных биоритмов по причине ночных пробуждений может провоцировать расстройство сна и усугублять уже имеющуюся ноктурию [5].
В одном из последний исследований авторы отметили антидиуретический эффект после приема снотворного препарата небензодиазепиновой структуры – золпидема. Помимо влияния на ночную продукцию мочи, препарат увеличивает ночной объем мочевого пузыря. Данные положительные эффекты были опосредованы повышением выработки минералокортикоидов, а также стабилизацией ГАМК-ергической системы, результатом которой являлось снижение афферентной передачи импульсов от мочевого пузыря к подкорковым структурам головного мозга [6].
Вышеописанные особенности этиопатогенеза ночного мочеиспускания, как наиболее значимого проявления СНМП, определяют поиск новых направлений медикаментозной коррекции.
Цель исследования – улучшение результатов лечения рефрактерной ноктурии путем комбинированной альфа-адренолитической и антиинсомнической терапии.
МАТЕРИАЛЫ И МЕТОДЫ
В основу анализа клинической эффективности комбинированной альфа-адренолитической и антиинсомнической терапии был положен опыт лечения и наблюдения за 65 больными с СНМП/ДГПЖ. Средний возраст пациентов составил 63,7±5 лет.
Количественную оценку СНМП производили, используя международную систему оценки симптомов при заболеваниях предстательной железы (IPSS) и опросник качества жизни (QоL).
Субъективные расстройства мочеиспускания объективно оценивались с помощью дневника, заполняемого в течение 2-3 дней до начала исследования, а затем на 8-ой неделе терапии. При его ведении фиксировалось и анализировалось количество суточных мочеиспусканий, в т. ч. дневных и ночных, эпизоды императивных позывов, ургентное недержание мочи, использование прокладок, объем выделенной мочи, объем потребляемой жидкости и диурез. Ночную полиурию определяли, если отношение ночного мочеобразования к суточному было более 33%. Ноктурию оценивали как состояние, характеризующееся необходимостью опорожнения мочевого пузыря два и более раз за ночь. Сопоставление показателей мочеобразования и мочевыделения выполняли с помощью расчета индекса ночной полиурии (ИНП) и ночного объема мочевого пузыря (ИНОМП).
Ультразвуковое исследование (УЗИ) мочевого пузыря, предстательной железы и верхних мочевых путей выполнялось на аппаратах «TOSHIBA-220 А» (Япония) и «Siemens Sienna» (Германия). Объем мочевого пузыря, остаточной мочи и предстательной железы (см³) автоматически вычислялся по формуле эллипса и выводился на монитор.
Урофлоуметрию проводили на аппарате «Urodin 1000» Medtronic (CША). Оценивали время и максимальную скорость мочеиспускания, объем выделенной мочи и тип урофлоуметрической кривой.
Оценку сна осуществляли при помощи Афинской шкалы бессонницы (Athens Insomnia Scale AIS), которая состоит из 8 вопросов. Определяли такие показатели как: субъективная оценка сна, нарушение засыпания, поддержание сна и др. Сумма баллов 5-11 интерпретировалась как легкая форма, 12-16 баллов – умеренная и 17-24 определялась как тяжелая бессоница.
Резюмируя вышеизложенное, критериями включения в исследование являлись:
- сохранение жалоб на ночные мочеиспускания, несмотря на проводимую ранее фармакологическую коррекцию тамсулозином (срок лечения не менее 2 месяцев);
- диагноз ДГПЖ I стадии на момент обследования;
- сумма баллов опросника IPSS от 7 до 19;
- концентрация общего ПСА в крови <4 нг/мл;
- Qmax ≥ 10 мл/с;
- объем предстательной железы по УЗИ до 40 см3;
- индекс ноктурии >1, индекс ночной полиурии >33%, индекс ночной емкости мочевого пузыря >0;
- наличие бессонницы (сумма баллов AIS ≥ 6).
Воспалительные заболевания верхних и нижних мочевых путей, гиперактивный мочевой пузырь, а также прием других лекарственных препаратов с целью коррекции инфравезикальной обструкции и бессонницы явились критериями исключения из исследования. Суточная полиурия, хроническая сердечная недостаточность II-III ст., гипертоническая болезнь III ст., хроническая болезнь почек являлись причиной невключения в исследование.
В качестве медикаментозной терапии были использованы селективный альфа-адреноблокатор – тамсулозин и снотворное средство небензодиазепиновой структуры – залеплон. Больные с AIS ≥ 6, страдающие бессонницей, были проконсультированы врачом-сомнологом и им был назначен двухмесячный курс приема залеплона.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
После комлексного обследования общей группы больных показано, что именно ноктурия является наиболее значимой жалобой среди всех СНМП у больных с ДГПЖ I стадии (рис.1).
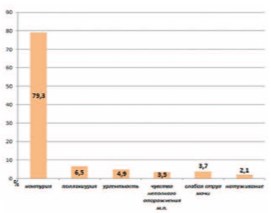
Рис. 1. Распределение жалоб при опросе больных с СНМП/ДГПЖ (%).
Частое ночное мочеиспускание, по мнению большинства опрошенных мужчин (79,3%), явилось основной причиной для обращения к врачу-урологу. Остальные жалобы на ирритативные и обструктивные расстройства мочеиспускания как приоритетные наблюдались у участников с частотой от 2,1 до 6,5%.
Анализируя этиологию ноктурии было выяснено, что изолированная ночная полиурия определялась у 10,5%, снижение ИНОМП – 38,1%, а сочетание данных причин – 51,4% пациентов.
Для изучения эффективности терапии рефрактерного ночного мочеиспускания при помощи альфаадреноблокатора и антиинсомнического препарата залеплона было выделено 31 лиц мужского пола, которые сформировали основную (первую) группу. В данной когорте больных назначался в капсульной форме тамсулозин и залеплон в суточной дозировке 0,4 мг и 5 мг соответственно. Альфа-адреноблокатор участниками исследования принимался утром после еды, в то время как антиинсомнический препарат был назначен за 30 минут до предполагаемого сна. Курс приема указанных препаратов составил 8 недель. Контрольную (вторую) группу составили 34 пациента, которые по аналогии получали тамсулозин в режиме монотерапии.
Оценку жалоб, данных дневника мочеиспускания, индексов расстройства мочеиспускания и сна, показателей уродинамики производили до начала и спустя 8 недель после лечения (табл. 1).
Таблица 1. Динамика показателей мочеиспускания на фоне комбинированной терапии больных СНМП/ДГПЖ и рефрактерной ноктурией, n=65
| Показатели | тамсулозин ( 0,4 n=34) | тамсулозин 0,4 мг + залеплон 5 мг (n=31) |
||
|---|---|---|---|---|
| до лечения | после лечения | до лечения | после лечения | |
| IPSS, баллы | 17,2±2,6 | 12,5±2,1a | 16,5±1,9 | 11,7±1,6a |
| QoL, баллы | 4,5±0,3 | 3,7±0,1 | 4,2±0,2 | 2,6±0,1a, b |
| Число ночных мочеиспусканий |
3,1±0,1 | 2,4±0,2 | 3,2±0,2 | 1,5±0,1a, b |
| Объем максимального мочеиспускания за сутки, мл |
230±45 | 360±50a | 220±55 | 390±35a |
| Объем остаточной мочи, мл | 45±15 | 35±10 | 74±15 | 35±10 |
| Максимальная скорость мочеиспускания, мл/с |
11,5±0,8 | 20,3±0,6a | 11,1±0,5 | 19,5±0,7a |
a – различие достоверно по сравнению с показателем до лечения (р<0,05);
b – различие достоверно по сравнению с показателем группы контроля (р<0,05)
У лиц, получающих альфа-адренолитическую терапию, отметили повышение максимальной скорости (с 11,5±0,8 до 20,3±0,6 мл/сек) и объема максимального мочеиспускания (с 230±45 до 360±50 мл), снижение баллов IPSS (с 17,2±2,6 до 12,5±2,1) и объема остаточной мочи (45±15 до 35±10 мл). Число ночных мочеиспусканий, сумма баллов по шкале QoL остались без значимых различий.
У участников, которым назначалась комбинированная терапия тамсулозином и залеплоном, по аналогии с предыдущей группой наблюдали увеличение показателя Qmax (с 11,1±0,5 до 19,5±0,7 мл/сек), объема максимального мочеиспускания (с 220±55 до 390±35), снижение баллов IPSS (с 16,5±1,9 до 11,7± 1,6) и объема остаточной мочи (74±17 до 35±10 мл). Однако, в отличие от первой группы, в данной когорте больных было отмечено достоверное снижение числа ночных мочеиспусканий (с 3,2±0,2 до 1,5±0,1) и суммы баллов опросника качества жизни (с 4,2±0,2 до 2,6±0,1) (р<0,05).
Кроме того, при использовании комбинированной терапии наблюдалось достоверное изменение индекса ночной полиурии с 34,9 до 25,2% (р<0,05) в отличие от группы лиц, принимавших альфа-адреноблокатор в режиме монотерапии, где данный показатель достоверно не различался (рис. 2).
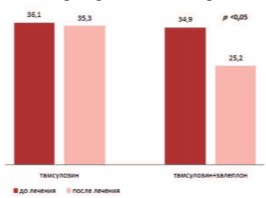
Рис. 2. Индекс ночной полиурии до и после терапии
Применение данной комбинации препаратов также привело к статистически значимому увеличению ночной емкости мочевого пузыря, которое было отражено в снижении индексе ночного объема мочевого пузыря с 1,5 до 0,8 (рис. 3).
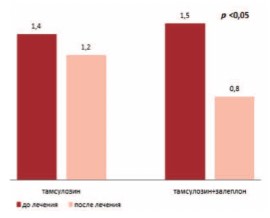
Рис. 3. Индекс ночного объема мочевого пузыря до и после терапии
Данные анкетирования опросника AIS до и после консервативной терапии представлены в таблице 2.
Таблица 2. Характеристика доменов AIS до и после лечения, n=65
| Домены AIS | тамсулозин ( 0,4 n=34) | тамсулозин 0,4 мг + залеплон 5 мг (n=31) |
||
|---|---|---|---|---|
| до лечения | после лечения | до лечения | после лечения | |
| Время засыпания, баллы | 1,5±0,2 | 1,6±0,3 | 1,4±0,1 | 0,6±0,1a, b |
| Ночные пробуждения, баллы | 2,5±0,3 | 2,1±0,2 | 2,2±0,3 | 1,1±0,2 a, b |
| Раннее утреннее пробуждение, баллы |
2,3±0,1 | 1,9±0,4 | 2,4±0,2 | 1,3±0,3 a, b |
| Общая продолжительность сна, баллы |
2,1±0,3 | 1,7±0,2 | 2,3±0,4 | 0,9±0,1 a, b |
| Общее качество сна, баллы | 2,5±0,2 | 2,1±0,3 | 2,2±0,3 | 1,2±0,3 a, b |
| Чувство «благополучия» в течение дня, баллы |
2,1±0,1 | 1,8±0,2 | 1,9±0,1 | 1,2±0,1 a, b |
| Функциональная активность в течение дня, баллы |
1,7±0,1 | 1,3±0,2 | 1,9±0,2 | 1,0±0,1 a, b |
| Сонливость в течение дня, баллы |
2,7±0,3 | 2,1±0,2 | 2,6±0,3 | 1,1±0,3 a, b |
| Общий балл | 17,4±1,8 | 14,6±2,0 | 16,8±1,8 | 8,4±1,5 a, b |
a – различие достоверно по сравнению с показателем до лечения (р<0,05);
b – различие достоверно по сравнению с показателем группы контроля (р<0,05)
По истечении восьми недель от назначения медикаментозной терапии произведена комплексная оценка всех компонентов опросника AIS. В группе мужчин, получавших комбинацию тамсулозина и залеплона, наблюдалось статистически достоверное снижение баллов всех доменов опросника. Суммарный средний балл AIS во второй группе снизился с 17,4±1,8 до 14,6±2,0; в первой – с 16,8±1,8 до 8,4±1,5 баллов (р<0,05). Данный показатель также различался после проведения терапии между двумя когортами (р<0,05).
В данном исследовании показано, что монотерапия тамсулозином эффективна в отношении только лишь обструктивной и ирритативной симптоматики у лиц, страдающих ДГПЖ и инсомнией. Тем не менее, отмечена низкая клиническая эффективность препарата данной группы в отношении частого ночного мочеиспускания. Наличие бессонницы является фактором, обусловливающим недостаточную эффективность альфа-адренолитической терапии. Использование опросника AIS позволяет определить нарушения сна как одну из вероятных причин рефрактерной ноктурии. Кроме того, после приема залеплона в сочетании с тамсулозином отмечено снижение ночной продукции мочи, а также повышение ночной емкости мочевого пузыря в ночное время суток.
ВЫВОД
Назначение тамсулозина в комбинации с залеплоном зарекомендовало себя как эффективный и безопасный фармакологический способ лечения резистентного ночного мочеиспускания у лиц с доброкачественной гиперплазией предстательной железым и инсомнией.
ЛИТЕРАТУРА
1. Kaplan SA. Reasons for prescription change of α1-blockers in patients with lower urinary tract symptoms suggestive of benign prostatic hyperplasia. J Urol 2015;193(4):1317.
2. Okada TY, Matsumoto K, Sumiyoshi T, Masuda N, Shiraishi Y, Negoro H, et al. The impact of lower urinary tract symptoms on generic health-related quality of life in male patients without co-morbidity. Nihon Hinyokika Gakkai zasshi 2015;106 (3):172-177.
3. Yazici CM, Kurt O. Combination therapies for the management of nocturia and its comorbidities. Res Reр Urol 2015;7:57-63.
4. Van Kerrebroeck P, Abrams P, Chaikin D. The standartization of terminology in nocturia: report from the standartization subcommittee of the International Continence Society. BJU Int 2002;90(3):11-15.
5. Drake M, Mills IW, Noble JG. Melatonin pharmacotherapy for nocturia in men with benign prostatic enlargement. J Urol 2004;171:1199-1202.
6. Yokoyama O, Matsuta Y, Yanai-Inamura H. Zolpidem increases bladder capacity and decreases urine excretion in rats. Neurourol Urodyn 2010;29:587-591.