Рудин Ю.Э., Марухненко Д.В., Алиев Д.К., Чекериди Ю.Э.
Эписпадия - редкий врожденный порок развития полового члена, входящий в единый комплекс пороков: экстрофия мочевого пузыря и эписпадия. Заболевание встречается 1:100 000 новорожденных и характеризуется расщеплением, незаращением дорсальной стенки уретры на различном протяжении. Соотношение мужской и женской эписпадии составляет 5:1. Данная патология может сочетаться с другими аномалиями: экстрофией мочевого пузыря, крипторхизмом, паховой грыжей. Выделяют головчатую, венечную, стволовую, субтотальную и тотальную форму эписпадии. Все мальчики с экстрофией мочевого пузыря имеют тотальную эписпадию. Головчатая, венечная и среднестволовая формы эписпадии не имеют нарушений удержания мочи и чаще всего не сопровождаются грубой деформацией кавернозных тел. Субтотальная форма сопровождается частичным неудержанием мочи. При тотальной форме эписпадии и экстрофии мочевого пузыря отмечается расщепленная головка, полностью открытый мочеиспускательный канал по дорсальной поверхности, крайняя плоть также расщеплена и локализуется преимущественно в области уздечки по вентральной поверхности. Лонные кости не соединены между собой, расстояние между ними может достигать 3-4 см, при экстрофии до 5-8 см (рис. 1). Дети с тотальной эписпадией имеют открытый сфинктер мочевого пузыря, полное недержание мочи с постоянным выделением ее наружу. Как следствие недержания мочи мочевой пузырь имеет малый объем и истонченную стенку. Половой член у больных с эписпадией значительно уменьшен в размерах, у детей с экстрофией мочевого пузыря половой член укорочен в среднем на 50% от нормальных величин и имеет выраженную дорсальную деформацию (член постоянно направлен вверх и в состоянии эрекции прижимается головкой к передней брюшной стенке) [1].
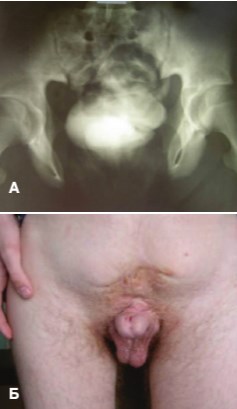
Рис.1 Пациент М., 17 лет. А. Диастаз расхождения лонных костей 12см. Б. Укорочение длины члена на 50% (5-7см)
Коррекция эписпадии предусматривает создание протяженного герметичного мочеиспускательного канала, достаточной ширины без сужений и мочевых свищей, устранение дорсальной деформации кавернозных тел без укорочения их длины и формирование анатомически правильной головки полового члена с наружным отверстием уретры на вершине. Хирургическое лечение тотальной и субтотальной форм эписпадии, сопровождающихся недержанием мочи, также предусматривает выполнение пластики шейки мочевого пузыря.
Традиционные методики лечения эписпадии, включая операции Cantwell-Ransley, Mitchell-Bagli, Du-play и Young привели к доказанному улучшению результатов реконструкции уретры и удлинению полового члена с улучшенными косметическими результатами [2]. Однако отдаленные результаты лечения показывают, что у каждой методики существуют определенные недостатки: укорочение ствола полового члена и сохранение деформации кавернозных тел, риск интраоперационного повреждения сосудистонервного пучка, частое возникновение свищей уретры и неудовлетворительный косметический результат [3].
Целью нашего исследования является разработка комплекса мер необходимых для полноценной коррекции эписпадии - формирование уретры, устранение деформации и удлинение кавернозных тел в сочетании с улучшением удержания мочи у детей с эписпадией и экстрофией мочевого пузыря.
МАТЕРИАЛЫ И МЕТОДЫ
В период с 2000 по 2014 гг. нами прооперировано 110 пациентов с эписпадией и экстрофией в возрасте от 5 дней до 18 лет. Операции новорожденным проводили на базе отделения новорожденных детской клинической больницы Св. Владимира (гл. врач. Попов В.В). Больных с эписпадией было 51: субтотальная эписпадия - у 27 детей, тотальная эписпадия - у 24. Экстрофия мочевого пузыря имелась у 57 пациентов, и с экстрофией клоаки было 2 мальчика. Условно все пациенты были разделены на три группы.
В первую группу вошли 10 пациентов, прооперированных в период с 2000 по 2006 гг. по поводу эписпадии в различных клиниках Москвы и России по методике Du-play. Этим больным формировали только мочеиспускательный канал, мобилизация кавернозных тел не проводилась, не выполняли иссечения рубцовой хорды и расправления кавернозных тел. Больным с экстрофией мочевого пузыря не предпринимались попытки сведения костей таза в области лонного сочленения, поскольку остеотомии таким детям не выполняли.
Вторую группу составили 18 детей, операции которым выполнены в период с 2006 по 2010 гг. Пациентам проведена пластика уретры по методике Cantwell с мобилизацией кавернозных тел, перемещением созданной уретры под кавернозные тела, в сочетании с операцией по сведению лонных костей и пластикой шейки мочевого пузыря. Однако отделения ножек кавернозных тел от ветвей лонных костей и пластики белочной оболочки по дорсальной поверхности полового члена не выполняли.
В третью группу включены 82 мальчика, которым проведен весь комплекс мер направленных на увеличение длины кавернозных тел полового члена. Пациенты оперированы в период с 2010 по 2014 гг. 32 больных имели эписпадию и 50 - экстрофию мочевого пузыря, возраст пациентов колебался от 1 года до 19 лет. (Средний возраст 4,36 лет).
Всем больным выполняли следующие обязательные исследования: клинический анализ крови, определение группы крови, резус-фактора, биохимический анализ крови, коагулограмма, ЭКГ, общий анализ мочи. Всем пациентам, способным удерживать мочу, проводилась урофлоуметрия для оценки качества мочеиспускания до и после операции. Выполнялось ультразвуковое исследование органов мочеполовой системы для исключения сочетанной патологии. Некоторым пациентам по показаниям выполнялись дополнительные исследования: цистография и экскреторная урография, цистоуретроскопия.
Особое внимание уделялось оценке внешних проявлений порока развития, анатомических особенностей и функциональному состоянию полового члена. Измеряли длину полового члена, положение меатуса (при эписпадии), ширину и длину уретральной площадки, определяли форму и диаметр наружного отверстия уретры. Длина пениса измерялась с помощью линейки, от пенопубитального угла до вершины головки в максимально натянутом положении (рис. 2).

Рис.2. Измерение длины кавернозных тел у больного В. 10 лет с субтотальной эиспадией и укорочением полового члена
Исходное функциональное состояние полового члена устанавливали, ориентируясь на данные анамнеза со слов родителей (частота и качество утренних спонтанных эрекций). Оценить степень деформации кавернозных тел при эписпадии достаточно сложно, а у мальчиков младшего возраста в особенности, поскольку спонтанные эрекции возникают довольно редко из-за низкого уровня тестостерона. Полноценную артифициальную эрекцию удавалось достигнуть только под общим наркозом, во время операции путем заполнения кавернозных тел физиологическим раствором. Для объективной оценки степени деформации кавернозных тел мы использовали транспортир. Углом деформации полового члена считали градус отклонения головки полового члена от ее нормального положения (рис. 3).
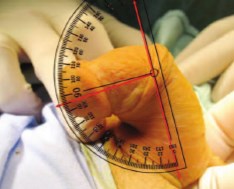
Рис. 3 Измерение угла деформации кавернозных тел у больного А. 16 лет с субтотальной эписпадией и 950 дорсальной деформацией кавернозных тел
Оперативное лечение: Нами предложен комплекс мер, направленных на устранение всех причин влияющих на укорочение длины кавернозных тел у больных с эписпадией и экстрофией.
Для мальчиков с экстрофией мочевого пузыря комплексный подход предусматривал несколько этапов лечения:
1 этап. Первичное закрытие дефекта мочевого пузыря. При операции закрытия мочевого пузыря у новорожденных детей в первые 3-5 дней после рождения наибольшее значение имеют:
- мобилизация кавернозных тел от седалищных костей на протяжении 2-3 см;
- максимально близкое сведение и фиксация лонных костей.
Выполнение операций в новорожденном возрасте обусловлено большей подвижностью и эластичностью костей таза, что позволяет надежно соединить лонные кости без остеотомий. Однако какой бы реконструктивный метод не применялся для закрытия или адаптации таза в раннем детстве, симфиз будет всегда повторно открываться со временем, что обусловлено недоразвитием (гипоплазией) с укорочением лонных костей и отставанием их роста в дальнейшей жизни [4]. Если оптимальные сроки для операции в новорожденном периоде были упущены, мы выполняли закрытие мочевого пузыря с двусторонней подвздошной остеотомией по Chiari силами наших коллег ортопедов-травматологов. Отломки тазовых костей в зоне остеотомии фиксировали с помощью спиц Киршнера и накладывали иммобилизирующую кокситную гипсовую повязку на 1-1,5 мес.
2 этап. Формирование уретры и расправление кавернозных тел. Важными этапами этой операции мы считаем:
- полное выделение кавернозных тел от рубцовой хорды;
- иссечение диспластичной спонгиозной ткани уретры;
- удлинение кавернозных тел за счет пластики белочной оболочки:
- методом нанесения поперечных насечек по дорсальной поверхности,
- методом графтинга (вставки), если нанесения насечек недостаточно для полного расправления кавернозных тел;
- выполнение максимально полной мобилизации уретральной площадки от вершины головки до основания кавернозных тел, позволяющей соотнести длину создаваемой уретры с длиной кавернозных тел;
- выполнение максимальной мобилизации ножек кавернозных тел от седалищных костей;
- создание герметичной уретры достаточной ширины тубуляризированным кожным лоскутом;
Для улучшения результатов лечения, в качестве предоперационной подготовки применялись инъекции хорионического гонадотропина человека и местные аппликации препарата тестостерона и дигидротестостерона короткими курсами 7-10 дней, что способствовало кратковременному увеличению длины полового члена в среднем на 2530% и улучшению кровообращения кавернозных тел, кожи ствола полового члена и крайней плоти [5]. Больший размер члена позволяет лучше выполнить все этапы операции мобилизовать кавернозные тела, выделить уретральную площадку, сформировать уретру, выполнить пластику крайней плоти, укрыть уретру и ушить послеоперационную рану на стволе члена без натяжения [6].
Мы использовали модификацию пластики уретры по Cantwell, считаем ее наиболее эффективной для удлинения и устранения деформации кавернозных тел и предупреждения послеоперационных осложнений. Суть данной техники заключается в выделении кавернозных тел от уретральной площадки. Кавернозные тела освобождают на всем протяжении от основания вплоть до вершины, однако отделения кавернозных тел от головки не проводят. Таким образом, пенис разделяется на составные части: правое и левое кавернозные тела, уретральная площадка с подлежащим спонгиозным телом, правая и левая сосудисто-нервные ножки (a. dorsalis penis, n. dorsalis penis.) (рис. 4) [7]. Важно помнить, что при экстрофии и эписпадии положение сосудисто-нервного пучка идет не по дорсальной, а по наружной (боковой) поверхности белочной оболочки кавернозного тела. Сосудистонервный пучок должен быть обязательно визуализирован и сохранен при выделении кавернозного тела для предупреждения некроза головки полового члена и эректильной дисфункции.
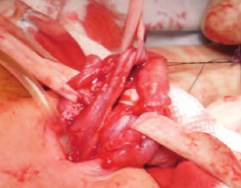
Рис. 4 Полное выделение уретральной площадки до вершины головки
3 этап. Пластика шейки мочевого пузыря для создания удерживающего механизма. Во время первичного закрытия мы всегда выполняем пластику шейки мочевого пузыря. Создается препятствие оттоку мочи из сформированного мочевого пузыря, что при хорошем заживлении раны и сформированной шейке обеспечивает рост мочевого пузыря, увеличение его объема, это приводит к увеличению времени «сухих промежутков». Это особенно важно у детей с малыми размерами пузырной площадки (микроцистисом). Однако не всегда удается добиться хорошего заживления раны. Нередко (25%) возникает несостоятельность швов на шейке мочевого пузыря. Не удается добиться полного удержания мочи [8]. Поэтому с целью улучшения качества жизни и социальной адаптации пациентам с недержанием мочи, выполняли повторную пластику шейки мочевого пузыря по методике Kelly с двусторонней надацетабулярной остеотомией. Выполнялась и мобилизация ножек кавернозных тел. Больным с субтотальными формами эписпадии и сохраненным удержанием мочи проводился лишь второй этап данного комплекса - формирование уретры и расправление кавернозных тел.
РЕЗУЛЬТАТЫ
Отдаленные результаты прослежены в сроки от 6 месяцев до 14 лет (табл. 1).
Таблица 1. Отдаленные результаты лечения в различных группах больных
| Группы больных | Хороший результат | Удовлетворительный результат | Отрицательныйрезультат |
|---|---|---|---|
| 1 группа (n=10) | 2 (1,8%) | 2 (1,8%) | 6 (5,5%) |
| 2 группа (n=18) | 8 (7,3%) | 3 (2,7%) | 7 (6,4%) |
| 3 группа (n=82) | 59 (53,6%) | 7 (6,4%) | 16 (14,5%) |
| ВСЕГО: | 69 (62,7%) | 12 (10,9%) | 29 (26,4%) |
Хорошим результатом считали следующие показатели характеризующие эффективность проведенного лечения.
1. Полное заживление послеоперационной раны и отсутствие подтекания мочи в виде свищей уретры;
2. Свободное мочеиспускание, с нормальными показателями урофлоуметрии;
3. Отсутствие деформации кавернозных тел (ровный половой член во время эрекции);
4. Отсутствие кожных подвесков, деформирующих кожных рубцов на стволе полового члена, наружное отверстие уретры на вершине головки (адекватный косметический результат);
Хороший результат отмечен у 69 пациентов (62,7%). Из них 2 ребенка из первой, 8 - из второй и 59 детей - из третьей группы.
Удовлетворительным результатом считали показатели умеренного нарушения потока мочи, смещение наружного отверстия на основание головки, остаточную деформацию кавернозных тел до 15 градусов (не влияющую на репродуктивную функцию) и рубцы кожи на стволе полового члена. Таких больных было 12 (10,9%).
Отрицательный результат в виде свищей уретры, стриктуры уретры и деформации кавернозных тел были получены у 29 больных (26,4%) на этапах лечения. Эти дети были в последующем повторно оперированы.
Анализ послеоперационных осложнений представлен в таблице 2. Наиболее часто в качестве осложнения мы наблюдали свищ уретры у 11 больных (10%). Подтекание мочи из сформированной уретры наблюдали чаще у больных 1 и 2 группы. Сужение уретры выявлено у 9 пациентов (8,2%). Это осложнения также чаше выявляли у больных 1-ой и 2ой группы. Остаточная деформация кавернозных тел обнаружена у 8 мальчиков (7,3%), дивертикул уретры сформировался у одного ребенка (0,9%) из 1-ой группы. Свищи уретры у 11 больных были ушиты путем реконструкции уретры. Двум больным дважды проводилось ушивание свища уретры. Стеноз уретры наблюдали у 9 мальчиков (8,2%). Один ребенок имел предстенотический дивертикул уретры, который был иссечен при повторной операции. Эндоскопическое рассечение зоны сужения уретры выполнено 5 больным с хорошим эффектом. Трем пациентам (4,5%) проведена пластика уретры с имплантацией свободного лоскута крайней плоти или слизистой щеки (двум пациентам) в область сужения.
Таблица 2. Характер осложнений в зависимости от метода лечения эписпадии
| Группа пациентов | Характер осложнений | ||||
|---|---|---|---|---|---|
| Свищ уретры | Стриктура уретры | Деформация кавернозных тел | Дивертикул уретры | Число осложнений | |
| 1группа (пластика уретры по Duplay, без сведения костей лона) n=10 | 2 (20%) | 2 (20%) | 1 (10%) | 1 (10%) | 6 (60%) |
| 2группа (пластика уретры по Cantwell + сведение лонных костей) n=18 | 3 (16,7%) | 2 (11,1%) | 2 (11,1%) | 0 (0%) | 7 (38,9%) |
| 3группа (этапное лечение) n=82 | 6 (7,3%) | 5 (6,1%) | 5 (6,1%) | 0 (0%) | 16 (19,5%) |
| Всего n=110 | 11 (10%) | 9 (0,8%) | 8 (7,3%) | 1 (0,9%) | 29 (26,4%) |
Отдельно оценивалась длина полового члена в состоянии эрекции или при максимальном растяжении кавернозных тел в длину. Известно, что средняя длина полового члена у взрослых мужчин, оперированных по поводу экстрофии, составляет 50% от нормы [9,10]. В нашем исследовании при оценке длины кавернозных тел у пациентов 1-ой группы средняя длина члена была 55% от нормы (6-7см) во взрослом состоянии. У больных 2-ой группы отмечалось увеличение показателей длины кавернозных тел (средняя длина 65% от нормы), у пациентов из третьей группы средняя длина составила 75-85% от нормы (табл. 3).
Таблица 3. Длина полового члена (см) у больных с эписпадией через 6 месяцев после хирургического лечения
| Возраст | Норма ±SD | 1 группа | 2 группа | 3 группа |
|---|---|---|---|---|
| Новорожденные | 3,0 ± 0,4 | - | - | - |
| 0-5 мес | 3,9 ± 0,8 | - | - | - |
| 6-12 мес | 4,3 ± 0,8 | - | - | - |
| 1 -2 года | 4,7 ± 0,8 | - | 3,3 | 3,7 |
| 2-3 года | 5,1 ± 0,9 | - | 3,6 | 4,4 |
| 3-4 года | 5,5 ± 0,9 | - | 3,8 | 5 |
| 4-5 лет | 5,7 ± 0,9 | - | 4 | 5 |
| 5-6 лет | 6,0 ± 0,9 | - | 4,2 | 4,8 |
| 6-7 лет | 6,1 ± 1,0 | 3,9 | 4,2 | 4,8 |
| 7-8 лет | 6,2 ± 1,0 | 3,7 | 4,2 | 4,8 |
| 8-9 лет | 6,3 ± 1,0 | 3,8 | 4,3 | 5 |
| 9-10 лет | 6,3 ± 1,0 | 3,8 | 4,4 | 5 |
| 10-11 лет | 6,4 ± 1,1 | 3,7 | 4,5 | 5 |
| Взрослые | 13,3 ± 1,6 | 7,3 | 9 | 10,5 |
В качестве примера приводим результаты операции у больных различных групп. На рисунке 1 представлен пациент 17 лет с экстрофией мочевого пузыря из 1-ой группы, которому не выполняли ни остеотомий, ни сведения лонных костей. Как видно на цистограмме, диастаз костей лонного сочленения составляет 12 см. При этом отмечается заметное укорочение полового члена (длина члена 5-7см).
Больному К., 12лет из 2-ой группы выполнена пластика шейки мочевого пузыря с двусторонней надацетабулярной остеотомией, сведением и фиксацией лонных костей. На рентгенограмме костей таза диастаз лонных костей составил 4 см, отмечено, увеличение длинны полового члена (рис. 5).
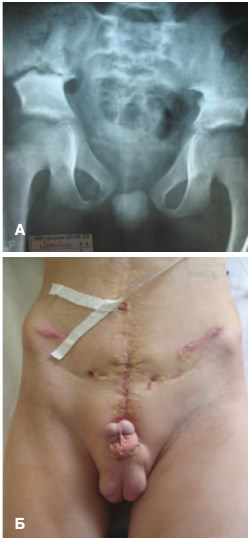
Рис. 5. Пациент К., 12 лет. А. Рентгенограмма костей таза через 4 недели после операции, видны зоны подвздошной остеотомии с обеих сторон. Б. отмечено увеличение кавернозных тел (8-9 см)
ОБСУЖДЕНИЕ
Накопленный нами опыт лечения пациентов с эписпадией и экстрофией мочевого пузыря позволил установить основные факторы определяющие длину кавернозных тел:
- исходная длина кавернозных тел (врожденная);
- диастаз лонных костей;
- степень мобилизации ствола и ножек кавернозных тел;
- степень дорсальной деформации кавернозных тел за счет гипоплазии белочной оболочки по дорсальной поверхности;
- длина артифициальной уретры (у ранее оперированных больных).
На рисунке 6А представлена схема положения кавернозных тел у пациента с экстрофией мочевого пузыря и диастазом костей лонного сочленения. За счет расхождения лонных костей наблюдается растяжение ножек кавернозных тел в стороны, тем самым укорачивается длина пениса. На рисунке 6Б стрелками указано направление мобилизации ножек кавернозных тел, что способствует удлинению полового члена. На рисунке 6В продемонстрировано, что при сведении лонных костей длина полового члена еще больше увеличивается. Очень важным моментом во время операции для первичного закрытия экстрофированного мочевого пузыря является максимальное сведение костей лона и фиксация их в таком положении. Без двусторонней остеотомии костей таза это удается успешно сделать только у новорожденных в первые 5-10 дней после рождения. Если эти сроки упущены, наилучшие результаты первичного закрытия мочевого пузыря при экстро-фии можно добиться, выполняя двустороннюю подвздошную надацетабулярную остеотомию по Chiari [11,12].
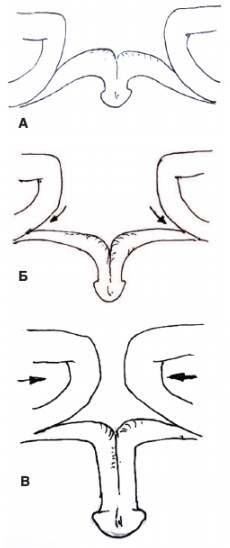
Рис. 6. Схема отражающая прямую зависимость длины кавернозных тел от диастаза лонных костей и степени мобилизации ножек кавернозных тел от лонных костей
Существует несколько вариантов мобилизации ножек кавернозных тел: без отсечения от лонных костей и полного отсечения ножек кавернозных тел от места их прикрепления к костям. Последний вариант предложили J.H. Kelly и соавт. в 1971 (рис.7) [13]. Однако нужно знать, что отсепаровка ножек кавернозных тел от кости может повлечь за собой повреждение (пересечение) сосудисто-нервных пучков полового члена, что приводит к ишемии и некрозу головки полового члена и импотенции. Поэтому, автор предложил отделять кавернозные тела вместе с частью надкостницы, тем самым сохраняя сосуды и нервные стволы полового члена. Данная методика успешно используется нами последние три года.
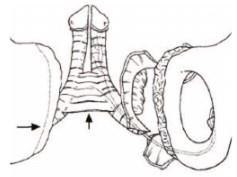
Рис.7. Схема периостальной мобилизации ножек кавернозных тел
Еще одним фактором, влияющим на длину кавернозных тел, является степень их дорсальной деформации. У больных с эписпадией и экстрофией имеется деформирующая хорда (зачаток порочной спонгиозной ткани уретры расположенной по дорсальной поверхности в области уретральной площадки). Существуют данные патоморфологических исследований, выявившие отклонения в строении белочной оболочки дорсальной порции кавернозных тел у больных с экстрофией и эписпадией [14]. Явления гипоплазии, разрастания соединительной ткани считают причиной медленного роста и укорочения длины белочной оболочки кавернозных тел по дорсальной поверхности, сохранения дорсальной деформации. Для увеличения ее длины нами предложена модификация операции, заключающаяся в выполнении множественных поверхностных поперечных насечек белочной оболочки по дорсальной поверхности. Это позволяет добиться выпрямления полового члена за счет удлинения дорсальной части кавернозных тел (рис.8). В случае грубых рубцовых изменений белочной оболочки, когда нанесенных насечек оказывается недостаточно, мы выполняем пластику белочной оболочки со вставкой свободного лоскута препуция по типу «графтинга». Суть метода заключается в выполнении двух параллельных Н-образных разрезов на дорсальной поверхности белочной оболочки. При тракции и мобилизации кавернозного тела вверх Н-образный разрез превращается в дефект белочной оболочки квадратной формы, который закрывают свободным лоскутом внутреннего листка крайней плоти [15]. При выраженной деформации и длинных кавернозных телах требуется аугментация белочной оболочки 4 лоскутами «графтами», по 2 на каждое кавернозное тело (рис. 9).
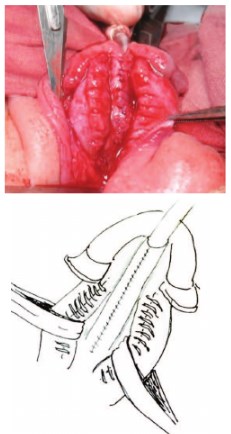
Рис.8. Схема нанесения поверхностных поперечных насечек на белочную оболочку кавернозных тел по дорсальной поверхности
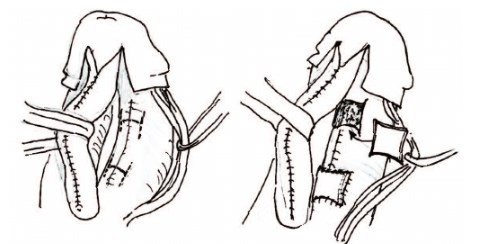
Рис.9. Схема аугментирующей пластики белочной оболочки путем «графтинга» - вшивания квадратных свободных лоскутов кожи крайней плоти в рассеченную белочную оболочку дорсальной поверхности кавернозных тел
Наш опыт показал, что для полного расправления кавернозных тел необходимо обеспечить максимальное удлинение уретральной площадки это возможно при полном выделении головчатого отдела уретры, для того чтобы длина соответствовала длине кавернозных тел. Мобилизация уретральной площадки в области головки позволяет увеличить длину уретры дополнительно на 4-8 мм. За счет этого имеется возможность избежать перемещения уретры на вентральную поверхность в области венечной борозды (гипоспадического меатуса). Кроме того, удается сформировать анатомически более правильный вариант наружного отверстия уретры на вершине. Важным моментом при этом является сохранение соединения между головкой, кавернозными телами и уретральной площадкой, в отличие от полного «дизэмблинга», применяемого при операции Perovic [14] или Mitchell-Bagli [16], когда половой член разделяется на кавернозные тела, рассеченные на всем протяжении, с соответствующими половинками головки и уретральную площадку. Тем самым удается сохранить более адекватное кровоснабжение головки и дистальной части создаваемой уретры, снижая при этом риск возникновения осложнений в виде стеноза меатуса, обусловленного ишемией тканей мобилизованной уретральной площадки, и образования свищей.
У ранее оперированных больных на степень деформации члена может влиять укорочение уретры, когда длина мобилизованных кавернозных тел оказывается больше длины ранее сформированной уретры. В таких случаях для полного расправления кавернозных тел требуется аугментация (увеличение длины уретры). С этой целью мы использовали у двух больных пластику уретры поперечным тубуляризированным лоскутом крайней плоти на сосудистой ножке.
ВЫВОДЫ
1. Выявление всех факторов влияющих на длину кавернозных тел при эписпадии и экстрофии, позволяет определить пути наиболее радикальной коррекции данного порока развития.
2. Пациентам с экстрофией мочевого пузыря показано выполнение первичного закрытия мочевого пузыря вместе со сведением и фиксацией лонных костей, с мобилизацией ножек кавернозных тел от седалищных костей. В случае если этого не было сделано в раннем новорожденном периоде, показано выполнение данной операции в сочетании с двусторонней подвздошной остеотомией по Chiari.
3. Модификация пластики уретры по Cantwell в сочетании с множественными поверхностными поперечными насечками по дорсальной поверхности белочной оболочки и выделением уретральной площадки в области головки более предпочтительна, т.к. обеспечивает достаточную мобилизацию кавернозных тел и при этом сохраняется адекватное кровоснабжение дистальной части создаваемой уретры, снижая риск возникновения осложнений в виде ишемии тканей и образования свищей.
4. Предложенный комплекс мер по лечению эписпадии позволяет достичь оптимальных косметических и функциональных результатов, а также снизить частоту осложнений с 60% до 19,51%, а также распрямить кавернозные тела и увеличить длину полового члена на 20-25%.
ЛИТЕРАТУРА
1. Лопаткин Н.А., Люлько А.В. Аномалии мочеполовой системы. Киев. Здоровье, 1987. C. 331-332
2. Gearhart JP, Jeffs RD. The bladder exstrophy-epispadias complex. In Walsh PC, Campbell MF, eds. Campbell's Urology, 7th ed. Philadelphia, WB Saunders, 1998, P. 1939.
3. Hafez AT, El-Sherbiny MT, Shorrab AA, El-Mowafi H. Complete primary repair of bladder exstrophy in children presenting late and those with failed initial closure: single center experience. J Urol 2005;174(4 Pt 2):1549-1552.
4. Gearhart JP, Rink RC, Mouriqand P. Pediatric urology, 2nd edition. Philadelphia, Saunders Elsevier, 2010. P. 386-411.
5. Perovic SV, Vukadinovic V, Djordjevic ML, Djakovic NG. Penile disassembly technique for epispadias repair: variants of technique. J Urol 1999;162(3 Pt 2):1181-1184.
6. Surer I, Baker LA, Jeffs RD, Gearhart JP. The modified Cantwell-Ransley repair in exstrophy and epispadias: 10 year experience. J Urol 2001;164(3 Pt 2):1040-1042.
7. Cantwell FV. Operative treatment of epispadias repair by transplantation of the urethra. Ann Surg 1895;22(6):689-694.
8. Рудин Ю.Э., Марухненко Д.В., Чекериди Ю.Э., Рассовский С.В., Руненко В.И. Способы коррекции экстрофии мочевого пузыря у детей. Детская хирургия 2009;(4): 26-31
9. Jaureguizar E, Lobato R. Penile length in adult after bladder extrophy reconstruction.
J. Pediatric urology 2008;4(1):77.
10. Silver RI, Yang A, Ben-Chaim J, Jeffs R, Gearhart JP. Penile length in adulthood after exstrophy reconstruction. J Urol 1997;157(3): 999-1003.
11. Ransley PG, Duffy PG, Wollin M. Bladder exstrophy closure and epispadias repair. In: Spitz L, Nixon HH, eds. Operative Surgery. London: Butterworths; 1988:620-632.
12. Ашкрафт К.У, Холдер Т.М. Детская хирургия. СПб., ООО «Раритет-М», 1999, C.15-17
13. Kelley JH, Eraklis AJ. A procedure for lengthening the phallus in boys with exstrophy of the bladder. J Pediatr Surg 1971; 6(5):645-649.
14. Perovic SV, Djinovic RP New insight into surgical anatomy of epispadiac penis and its impact on repair. J Urol. 2008; Volume 179(2): 689-695.
15. Рудин Ю.Э. Патент на изобретение № 2429790. Способ хирургического лечения порока полового члена при эписпадии и экстрофии мочевого пузыря. URL: http://www1.fips.ru/wps/portal/IPS_Ru#1478808065125
16. Mitchell ME Bagli DJ. Complete penile disassembly for epispadias repair: the Mitchell technique. J Urol 1996;155(1):300-304.
Журнал «Экспериментальная и клиническая
урология» Выпуск №4 за 2016 год