Васильченко М.И., Погосян Р.Р., Забелин М.В., Семенякин И.В., Самойлов А.С., Сергеев В.П., Кызласов П.С.
C учетом увеличения заболеваемости раком мочевого пузыря во всем мире, а также расширением показаний к выполнению радикальной цистэктомии, остро ставится вопрос выбора метода отведения мочи [1,2]. Достигнутые в последние годы значительные успехи в области хирургического лечения различных заболеваний нижних мочевыводящих путей не исключают проблем, связанных с методом отведения мочи при цистэктомии. Они попрежнему остаются в центре внимания урологов и еще далеки от окончательного решения [3]. Золотым стандартом лечения мышечноинвазивного рака мочевого пузыря, который составляет до 25% от всех форм рака мочевого пузыря, является радикальная цистэктомия [4,5].
Применение сегмента тонкого кишечника за последнее время зарекомендовало себя как оптимальный метод деривации мочи. В некоторых случаях формирование ортотопического неоцистиса не представляется возможным по ряду причин: анатомически короткая брыжейка подвздошного кишечного трансплантата, при которой невозможно низведение сформированного неоцистиса в малый таз; распространенное опухолевое поражение тазового дна или органов малого таза и др. При таких условиях показано отведение мочи путем создания гетеротопического мочевого неоцистиса, либо использование других методов. Формирование удерживающего механизма при гетеротопической пластике мочевого неоцистиса позволяет улучшить качество жизни больных при отсутствии показаний для ортотопического варианта неоцистиса [6,7].
Цель исследования: изучение результатов хирургического лечения больных с органической патологией мочевого пузыря, требующей выполнения цистэктомии и деривации мочи посредством гетеротопической тонкокишечной пластики мочевого пузыря.
МАТЕРИАЛЫ И МЕТОДЫ
Изучены результаты хирургического лечения 105 больных с верифицированным диагнозом рака мочевого пузыря в стадии Т24N02M0х, которым была выполнена цистэктомия и деривация мочи. Пациенты наблюдались на клинической базе ГБУЗ МО «Московского областного онкологического диспансера» г. Балашиха, ГКБ №68 г. Москвы, ГКБ им. С.И. Спасокукоцкого г. Москвы. Мужчин было 93 (88,6%), женщин 12 (11,4%), возраст больных колебался от 65 до 80 лет. Больные были разделены по группам в зависимости от способа отведения мочи: гетеротопическая пластика мочевого пузыря по методу М.И. Васильченко и соавт. 35 (33,3%) больных; гетеротопическая тонкокишечная пластика мочевого неоцистиса по предложенной авторами методике 35 (33,3%) больных; операция илеокондуит по Bricker 35 (33,3%) пациентов.
Во всех случаях с целью создания кишечного неоцистиса (резервуара) использовался терминальный отдел подвздошной кишки, отступив от илеоцекального угла на 25 см, с обязательным сохранением а. ileocolica. Способ определения длины резекции тонкой кишки, предложенный И.В. Семенякиным и соавт. и используемый в данной работе, позволил выполнить экономную и обоснованную резекцию участка подвздошной кишки с целью создания необходимого объема артифициального мочевого пузыря [8].
Оригинальный способ гетеротопической пластики мочевого пузыря, предложенный И.В. Семенякиным, М.И. Васильченко и соавт. был нами модифицирован и применен с целью создания гетеротопического тонкокишечного мочевого неоцистиса. Техника выполнения была следующая: выкроенный сегмент подвздошной кишки на сосудистой ножке длиной до 55 см (обязательное сохранение а. ileocolica) складывают в виде буквы W, делят на участки в проксимальном и дистальном участках по 10 см каждый и между ними два участка по 20 см. Формирование тонкокишечного (артифициального) мочевого пузыря начинают путем сшивания задних стенок рассеченной кишки однорядным узловым швом. В состоянии умеренного натяжения по длине и ширине рассеченные и обращенные друг к другу края обоих двух колен сшивают непрерывным швом, рассасывающейся нитью. Сформированный кишечный лоскут затем складывают в большой резервуар, сшивая края кишечного лоскута создают переднюю стенку мочевого пузыря. Путем сшивания задних стенок рассеченной кишки, а затем сшиванием передней стенки, формируется резервуар для мочи с низким давлением (рис. 1). Мочеточники, после предварительной интубации, имплантируют по антирефлюксной методике. Далее при формировании стомы проксимальный конец недетубуляризированного участка мочевого пузыря выводится через разрез в левой подвздошной области.

Рис. 1. Резервуар для мочи с низким давлением
Вторым этапом после цистэктомии выполнялась резекция сегмента кишечника. В зависимости от планируемого объема мочевого неоцистиса (резервуара) применялся способ определения длины резекции тонкой кишки. По данным различных литературных источников, необходимо выделение протяженного участка мочеточников перед этапом формирования уретерокишечных анастомозов, т.к. в дальнейшем могут происходить трофические нарушения стенки мочеточника, что ведет к некрозу дистального отдела мочеточника, а также к несостоятельности уретерокишечных анастомозов [5]. Применение нами оригинальных методик формирования гетеротопического тонкокишечного мочевого неоцистиса (резервуара) позволяет исключить развитие данных осложнений, поскольку концы резецированного сегмента кишечника подводятся к дистальным отделам мочеточников, выделенных на протяжении не более 1525 мм, что полностью позволяет сформировать уретерокишечный анастомоз, сохранив полное кровоснабжение в культе мочеточника.
Способ создания гетеротопического тонкокишечного мочевого неоцистиса позволяет интраоперационно придать резервуару овоидную форму, которая в последующем приближается к шаровидной. Следующим этапом формируется удерживающий клапан на проксимальном конце мочевого неоцистиса (резервуара) с выведением стомы на переднюю брюшную стенку создание губовидного свища.
Рентгенологические методы диагностики мочевого неоцистиса (резервуара) позволяют оценить его форму, объем, а также состояние уретерокишечных анастомозов, уродинамику верхних мочевыводящих путей и удерживающего механизма стомы. Динамические радиологические методы исследования, выполненные у больных на разных сроках наблюдения в послеоперационном периоде, дают возможность оценить функцию почечной паренхимы, транспортировку радиофармпрепарата по реконструированному уретерокишечному анастомозу. Для изучения качества жизни больных использовали анкетирование с помощью специальных опросников (опросник SF36, опросник стомированного больного) на различных сроках после операции, функция удержания мочи оценивалась на основании терминологии ICS по классификации McGuire, способы опорожнения мочевого пузыря, а также функции удержания мочи по критериям Хаутманна.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Величина средней продолжительности оперативного лечения составила 358,1 (150700) минут. Интраоперационная кровопотеря, обусловленная технической сложностью выполнения цистэктомии, в среднем составила 365,1 (1501100) мл, при этом способ отведения мочи на объем кровопотери не оказывал влияния.
Максимальный срок наблюдения за пациентами составил 10 лет. Оценка результатов хирургического лечения проводилась по данным, полученным в ходе обследования пациентов через 14, 30 суток, 3, 6, 12 месяцев, 2 10 лет.
По результатам выполненной экскреторной урографии в ранние сроки после оперативного лечения (7 30 суток) определялись умеренные ретенционные изменения чашечнолоханочной системы почек у 10 (9,52%) из 105 пациентов (рис. 2). Обострение хронического пиелонефрита наблюдалось у 10 (9,52 %) больных, которым выполнялась деривация мочи путем формирования илеокондуита по Брикеру, после проведения консервативной антибактериальной терапии данный процесс был купирован.

Рис. 2. Экскреторная урография в ранние сроки после оперативного лечения
Сформированные гетеротопические тонкокишечные мочевые резервуары, по данным динамической ангионефросцинтиграфии в комплексе с другими методами исследования, позволили улучшить основные функции почек по сравнению с предоперационным состоянием. Анализ результатов динамической сцинтиграфии у 48 (46%) больных, произведенной через 3, 6, 12 мес. и 15 лет после операции формирования гетеротопического тонкокишечного мочевого резервуара, показал, что транспортировка радиофармпрепарата по реконструированному уретерокишечному сегменту в большинстве случаев не нарушена, функциональное состояние почечной паренхимы не ухудшалось. Также оценивалась функция почек в сопоставлении с состоянием верхних мочевыводящих путей до выполнения операции. У 89% больных в предоперационном периоде на фоне воспаления отмечены выраженные изменения в крови и моче, прогрессирование хронической почечной недостаточности (ХПН), электролитные нарушения. После шечнолоханочной системы у наблюдаемых больных приходили к нормальным значениям, не изменяясь в дальнейшем (рис. 3).
Рис. 3. Экскреторная урография через 1,5 месяца после операции
Таким образом, умеренные ретенционные изменения чашечнолоханочной системы почек, наблюдавшееся у 10 из 105 пациентов в раннем послеоперационном периоде, уже к 3 месяцам после операции были купированы полностью, не выявляясь в дальнейшем (рис. 4).
Рис. 4. Экскреторная урография через 3 месяца после операции
Сформированные гетеротопические тонкокишечные мочевые резервуары, по данным динамической ангионефросцинтиграфии в комплексе с другими методами исследования, позволили улучшить основные функции почек по сравнению с предоперационным состоянием. Анализ результатов динамической сцинтиграфии у 48 (46%) больных, произведенной через 3, 6, 12 мес. и 15 лет после операции формирования гетеротопического тонкокишечного мочевого резервуара, показал, что транспортировка радиофармпрепарата по реконструированному уретерокишечному сегменту в большинстве случаев не нарушена, функциональное состояние почечной паренхимы не ухудшалось. Также оценивалась функция почек в сопоставлении с состоянием верхних мочевыводящих путей до выполнения операции. У 89% больных в предоперационном периоде на фоне воспаления отмечены выраженные изменения в крови и моче, прогрессирование хронической почечной недостаточности (ХПН), электролитные нарушения. После проведенных операций на фоне интенсивной терапии с коррекцией электролитных нарушений, с учетом посевов мочи на флору и определением чувствительности к антибиотикам, явления воспаления купированы, в биохимических анализах крови отмечалась стабилизация или уменьшение показателей креатинина, мочевины, калия. Причем, снижение показателей было отмечено в первые три месяца послеоперационного периода. Исходно до операции уровень креатинина крови у пациентов в среднем составлял 150 ± 15,5 мкмоль/л, спустя 3 месяца после операции средний показатель составил 125± 10 мкмоль/л (рис. 5). Схожие изменения фиксировались и при определении уровня мочевины крови: до операции среднее значение мочевины крови являлось 12,3±3,2 ммоль/л, спустя 3 месяца после операции средний показатель составил 9,4 ± 2,5 мколь/л (рис. 6).
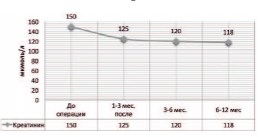
Рис. 5. Динамика изменения уровня креатинина в крови в различные сроки после операции
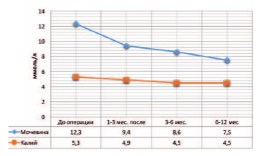
Рис. 6. Динамика изменения уровня мочевины и калия в крови в различные сроки после операции
В качестве примера улучшения функции почек приводим следующее клиническое наблюдение:
Пациент Н., 68 лет: в период подготовки к операции больному выполнена динамическая ангионефросцинтиграфия с целью определения фильтрационной функции почек и уродинамики верхних мочевыводящих путей. По результатам исследования определялся обтурационный тип кривой на ренограммах,
гемодинамика почек относительно удовлетворительная, фильтрационная функция почек снижена, ренограммы плоского обструктивного типа, выраженное снижение выделительной функции обеих почек. Снижение клиренсовой функции, признаки ХПН (рис. 7).
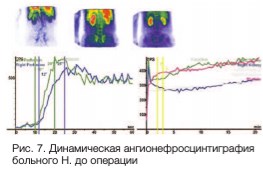
Рис. 7. Динамическая ангионефросцинтиграфия больного Н. до операции
Через 3 месяца после операции пациенту выполнено повторное исследование, по результатам которого отмечалось положительное влияние выполненной операции на функцию почек, слева паренхиматозный тип кривой, что свидетельствовало о восстановлении уродинанамики левой почки, справа отрицательной динамики не отмечается. Прогрессирования снижения гемодинамики и фильтрационной функции почек не отмечено, также как и нарастания признаков хронической почечной недостаточности (рис. 8).
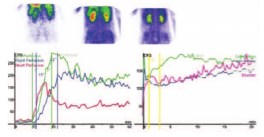
Рис. 8. Динамическая ангионефросцинтиграфия больного Н. через 3 месяца после операции
Рентгенрезервуарография подтвердила эффективность применяемой атирефлюксной методики создания уретерокишечных анастомозов. Во время тугого наполнения неоцистиса (резервура) у 70 больных, перенесших оригинальные методики формирования гетеротопических неоцистисов, рентгенологически отсутствовали рефлюксы в верхние мочевые пути (рис. 9).
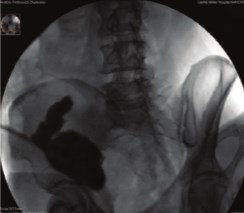
Рис. 9. Рентгенрезервуарография больного Н.
После удаления трубки из стомы у 35 (33,3%) из 105 оперированных больных, проведено исследование герметичности клапана и жома при натуживании и положении больного на животе, при этом оценивалось удержание мочи. Результаты исследований указывали на хорошую герметичность стомы в различные сроки послеоперационного периода (рис. 10).
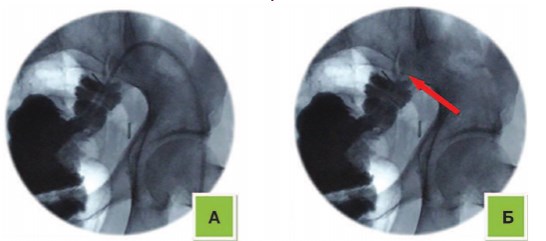
Рис. 10. Исследование герметичности клапана и жома: А при натуживании; Б в положении больного на животе
Резервуарография гетеротопического тонкокишечного мочевого неоцистиса у 43 больных, выполненная в различные сроки после операции, свидетельствовала, что формирование окончательного объема резервуара происходит в течение первого года после операции (табл. 1).
Таблица 1. Динамика изменения объема гетеротопического тонкокишечного мочевого пузыря (резервуара) по оригинальным методикам в послеоперационном периоде
| Сроки наблюдения | Объем гетеротопического мочевого резервуара с запланированным объемом (мл) | |||||||
|---|---|---|---|---|---|---|---|---|
| Гетеротопическая пластика мочевого резервуара по методу М.И. Васильченко и соавт. 300 мл (n=21) | Гетеротопическая тонкокишечная пластика мочевого неоцистиса (авторская методика) 350 мл (n=22) | |||||||
| 3 месяца | 210±23 | 319±14 | ||||||
| 6 месяцев | 290±12 | 327 ±12 | ||||||
| 1 год | 305±18 | 353±10 | ||||||
| 2 года | 310±7 | 372±7 | ||||||
| 3 года | 307 ±15 | 362±5 | ||||||
| 4 года | 324±19 | 371±10 | ||||||
Для оценки эффективности выполненных гетеротопических илеоцистопластик при обоснованном объеме резекции кишечника на уровень цианокобаламина (витамина В12) в послеоперационном периоде были обследованы две группы пациентов. В группу «А» вошли пациенты, которым выполнена операция илеокондуит по Bricker. В группу «Б» вошли больные, которым выполнена гетеротопическая пластика мочевого пузыря. Динамика изменения уровня Цианокобаламина представлена на рисунке 11. В группе «Б» уровень цианокобаламина практически не изменялся на протяжении всего срока после перенесенного оперативного вмешательства: средний уровень до операции составил 362±51 пг/мл и спустя 5 лет после оперативного лечения 333±28 пг/мл. Прогрессивное снижение уровня цианокобаламина отмечалось в группе «А» на протяжении 5 лет после перенесенного оперативного лечения от 416±29 пг/мл до операции до 179±23 пг/мл. Полученные данные указывают на то, что при необоснованно большой резекции кишечника происходит прогрессивное снижение уровня цианокобаламина в послеоперационном периоде, при этом снижение ниже уровня нормы происходит через 3 года после операции. Обнаружены статистически достоверные различия среднего уровня цианокобаламина в исследованных группах сравнения через 4 и 5 лет после оперативного лечения. Уровень цианокобаламина, при применении предложенного способа расчета длины оптимальной резекции кишечника, остается стабильным на протяжении 5 лет после операции, при этом практически не изменяется по сравнению с предоперационным уровнем, что может свидетельствовать об эффективности применяемого авторского способа.
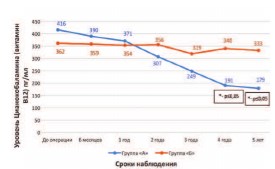
Рис. 11. Динамика изменения уровня Цианокобаламина (витамин В12)
Показатели электролитных изменений состава крови до и в различные сроки после операции исследованы в тех же группах больных (табл. 2). Полученные данные указывают на то, что прогрессивное снижение уровня натрия в сыворотке крови до 128,3±0,8 ммоль/л происходит через 1 месяц после оперативного лечения у пациентов группы «А». Восстановление уровня натрия до 136,0±1,2 ммоль/л в сыворотке крови отмечается лишь к 18ому месяцу после операции и в дальнейшем соответствует референсным значениям. Увеличение уровня калия в сыворотке крови у больных группы «А» до 4,58± 0,01 ммоль/л достигается через год после оперативного лечения, а в последующие годы не изменяется. Прогрессивное снижение уровня хлора в сыворотке крови до 87,8± 0,3 ммоль/л отмечено через 1 месяц после оперативного лечения, однако уже к 6ому месяцу уровень хлора в сыворотке крови становится выше референсных значений, практически не меняясь в дальнейшем. В группе «Б» уровень изучаемых показателей уже через 6 месяцев после операции соответствовал референсным значениям и не изменялся на протяжении всего срока наблюдения.
Таблица 2. Динамика электролитных изменений состава крови
| Сроки | Группа «А» | Группа «Б» | ||||
|---|---|---|---|---|---|---|
| Na (N=133142) ммоль/л | K (N=3,54,7) ммоль/л | Cl (N=97108) ммоль/л | Na (N=133142) ммоль/л | K (N=3,54,7) ммоль/л | Cl (N=97108) ммоль/л | |
| До операции | 133,8±1 1 | 3,60±0,01** | 100,5±1,2 | 134,2±0,8 | 3,92±0,04** | 100,5±0,9 |
| 1 месяц | 128,3±0,8* | 4,58±0,04** | 87,8±0,3*** | 131,3±1,0* | 3,81 ±0,06** | 95,2 ±1,3*** |
| 6 месяцев | 131,0±1,2 | 4,52±0,04** | 107,0±1,3 | 133,4±0,8 | 3,55±0,03** | 99,2±0,6 |
| 12 месяцев | 132,8±1 1 | 4,58±0,01** | 108,3±0,6 | 135,0±0,9 | 3,72±0,02** | 103,5±0,8 |
| 18 месяцев | 136,0±1,2 | 4,54±0,04** | 106,5±0,5 | 133,1±1,1 | 3,69±0,04** | 98,5±0,6 |
| 24 месяца | 136,3±0,7 | 4,31 ±0,02** | 104,8±0,6 | 135,1±1,2 | 3,71 ±0,02** | 98,2±0,6 |
| 36 месяцев | 137,1 ±0,5 | 3,48±0,02 | 106,1 ±0,4 | 133,0±0,4 | 3,60±0,01 | 100,2±0,2 |
| 48 месяцев | 134,0±1,2 | 3,68±0,01 | 106,2±0,2 | 134,4±0,2 | 3,62±0,02 | 98,6±0,5 |
*p ≤ 0,05 при сравнении уровня Na в группах на исследуемых сроках
** p ≤ 0,05 при сравнении уровня K в группах на исследуемых сроках
*** p ≤ 0,05 при сравнении уровня Cl в группах на исследуемых сроках
Проведенное исследование герметичности клапана и жома неоцистиса при натуживании у 35 больных свидетельствовало о полном удержании мочи последними, что обеспечило улучшение качества жизни пациентов, а также доказало эффективность создаваемого клапанного механизма.
В различные сроки после операции (14, 30 суток, 3, 6, 12 месяцев, 2 10 лет) было оценено качество жизни больных путем анкетирования. Установлено, что за счет сокращения числа аутокатетеризаций вследствие увеличения объема резервуара, достигается улучшение качества жизни пациентов: если в первые три месяца после операции больным приходилось выполнять самокатетеризацию через каждые 1,52 часа, то при увеличении объема «мочевого пузыря» к 4ому месяцу интервал между самокатетеризациями возрастал до 3,5 4 часов (рис. 12).
Рис. 12. Динамика количества самокатетеризаций гетеротопического тонкокишечного мочевого резервуара при увеличении его емкости
Для оценки и сравнения качества жизни больных после цистэктомии с различными видами кишечной деривации мочи было обследовано 105 пациентов. Все пациенты были разделены на группы.
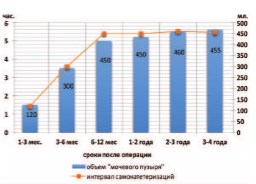
Рис. 12. Динамика количества самокатетеризаций гетеротопического тонкокишечного мочевого резервуара при увеличении его емкости
В группу «А1 » вошли 35 пациентов после гетеротопической пластики мочевого неоцистиса по авторской методике, 35 пациентов (группа «А2») после гетеротопической пластики мочевого резервуара по методу М.И. Васильченко и соавт. и 35 пациентов (группа «А3») после формирования илеокондита по Bricker.
Была сформирована контрольная группа (группа «К»), состоявшая из 35 мужчин (средний возраст 67,5 года), не страдающих онкологическими заболеваниями, прошедших тестирование по шкале IPSS и имеющих балл 56, QоL 02.
В качестве инструмента для оценки качества жизни была выбрана русская версия общего (неспецифического) опросника SF36.
С целью объективизации и стандартизации оценки качества жизни у больных, перенесших реконструктивные оперативные вмешательства на нижних мочевых путях использовался опросник SF36.
При сравнении полученных результатов контрольной группы (К) и группы пациентов, перенесших гетеротопическую пластику
мочевого пузыря (группы А1 и А2) отмечается снижение показателей в группе оперированных больных практически по всем шкалам. Наиболее выражено снижение показателей по шкале роль физических проблем в ограничении жизнедеятельности (RP), общее восприятие здоровья (GH), жизнеспособность (VT), роль эмоциональных проблем (RE) (табл. 3).
Таблица 3. Качество жизни у пациентов, перенесших гетеротопическую пластику мочевого пузыря, и контрольной группы
| Показатель | Группа «К» | Группа «А» | |
|---|---|---|---|
| «А1» | «А2» | ||
| PF-Физическая активность | 97,3±7,9 | 85,7±4,0 | 85,3±3,7 |
| RP-Роль физических проблем в ограничении жизнедеятельности | 84,3±11,7 | 47,5±3,0* | 48,0±2,6* |
| BP-Физическая боль | 85,3±8,1 | 77,9±4,2 | 76,8±4,0 |
| GH-Общее восприятие здоровья | 79,8±4,3 | 58,2±7,9* | 59,0±7,2* |
| VT-Жизнеспособность | 72,3±5,3 | 59,3±2,6 | 59,1±3,2 |
| SF-Социальная активность | 81,9±7,7 | 79,2±7,5 | 78,1±5,3 |
| RE-Роль эмоциональных проблем в ограничении жизнедеятельности | 83,2±11,5 | 27,3±4,7* | 25,9±5,1* |
| MH-Психическое здоровье | 70,1 ±3,2 | 65,1±2,5 | 64,9±2,3 |
| CH-Сравнение самочувствия с предыдущим годом | 56,5±6,1 | 51,8±2,4 | 50,4±2,2 |
*статистически достоверные различия (р<0,05) с контрольной группой
Отмечено достоверное снижение показателя общего восприятия здоровья (GH), эмоциональных проблем (RE). Вместе с тем, по таким шкалам как физическая активность (RF), физическая боль (BP), жизнеспособность (VT), социальная активность (SF), психическое здоровье (MH) и сравнение самочувствия с предыдущим годом (CH) разница результатов оказалась статистически не достоверной. Сравнивая результаты, полученные при анкетировании, выявлено, что принципиальных различий по всем показателям в группах пациентов после гетеротопических цистопластик по оригинальным методикам нет.
При сравнении полученных результатов контрольной группы (К) и групп пациентов перенесших гетеротопическую пластику мочевого неоцистиса по предложенной методике (А1) и операцию илеокондуит по Bricker (А3) отмечается снижение показателей оперированных больных практически по всем шкалам. Наиболее выражено снижение показателей по шкале роль физических проблем в ограничении жизнедеятельности (RP), общее восприятие здоровья (GH), жизнеспособность (VT) и максимально в шкале роль эмоциональных проблем (RE). Отмечено достоверное снижение показателя общего восприятия здоровья (GH), эмоциональных проблем (RE), физическая активность (RF). Вместе с тем, по таким шкалам как физическая боль (BP), жизнеспособность (VT) и сравнение самочувствия с предыдущим годом (CH) разница результатов оказалась статистически не достоверной. Но при сравнении показателей контрольной группы и группы пациентов с илеокондуитом по Bricker отмечается статистически достоверная разница значений в значениях социальная активность (SF) и психическое здоровье (MH). Результаты сравнения показателей контрольной группы и группы пациентов, перенесших гетеротопическую тонкокишечную пластику мочевого пузыря (предложенная методика), илеокондуит по Bricker представлены в таблице 4.
Таблица 4. Качество жизни у пациентов, перенесших гетеротопическую тонкокишечную пластику мочевого неоцистиса (предложенная методика), илеокондуит по Bricker и контрольной группы
| Показатель | Группа «К» |
Группа «А» | Р/Р1 | |
|---|---|---|---|---|
| «А1» | «А3» | |||
| PF-Физическая активность | 97,3±7,9 | 85,7±4,0 | 75,4±3,1 | >0,1 |
| RP-Роль физических проблем в ограничении жизнедеятельности | 84,3±11,7 | 47,5±3,0 | 41,2±4,3 | <0,05 |
| BP-Физическая боль | 85,3±8,1 | 77,9±4,2 | 80,3±3,3 | >0,1 |
| GH-Общее восприятие здоровья | 79,8±4,3 | 58,2±7,9 | 46,2±5,1 | <0,05 |
| VT-Жизнеспособность | 72,3±5,3 | 59,3±2,6 | 52,5±2,0 | >0,1 |
| SF-Социальная активность | 81,9±7,7 | 79,2±7,5 | 53,7±7,1 | >0,1/<0,05 |
| RE-Роль эмоциональных проблем в ограничении жизнедеятельности | 83,2±11,5 | 27,3±4,7 | 23,8±4,2 | <0,05 |
| MH-Психическое здоровье | 70,1 ±3,2 | 65,1 ±2,5 | 41,1 ±6,4 | >0,1/<0,05 |
| CH-Сравнение самочувствия с предыдущим годом | 56,5±6,1 | 51,8±2,4 | 47,9±2,7 | >0,1 |
*статистически достоверные различия (р<0,05) с контрольной группой
ВЫВОДЫ
Формирование гетеротопического тонкокишечного мочевого неоцистиса (резервуара) по предложенным нами методикам является достойной альтернативой известной ортотопической пластике. Благодаря наличию сформированного клапана и жома больные способны удерживать мочу, а созданные резервуары низкого внутрипросветного давления обладают достаточной емкостью и приводят к улучшению основных функций почек в динамике со сравнением с их предоперационным состоянием.
ЛИТЕРАТУРА
1. Аполихин О.И., Сивков А.В., Солнцева Т.В., Комарова В.А. Анализ урологической заболеваемости в Российской Федерации в 20052010 годах . Экспериментальная и клиническая урология 2012;(2): 39.
2. Матвеев В.Б., Волкова М.И., Фигурин КМ., Медведев С.В., Н1осов Д.А., Хмелевский Е.В., и др. Клинические рекомендации по диагностике и лечению больных раком мочевого пузыря. Ассоциация онкологов России. Москва. 2014, 32 с.
3. Переверзев A.C., Петров С.Б. Опухоли мочевого пузыря. Харьков: Факт. 2002, 304 с.
4. Stein JP, Skinner DG. Results with radical cystectomy for treating bladder cancer: a «reference standart» for highgrade, invasive bladder cancer. BJU Int 2003; 92(l):1217.
5. Stenzl A, Cowan NC, De Santis M, Jakse G, Kuczyk MA, Merseburger AS, et al. The updated EAU guidelines on muscleinvasive and metastatic bladder cancer. Eur Urol 2009;55(4):815825. doi: 10.1016/j.eururo.2009.01.002
6. Jimines VK, Marshall FF. Surgery of bladder cancer. In Campbell’s Urology [ed. by P.C. Walsh, A.B. Retic, E.D. Vaughan, A.J. Wein]. 8th ed. Philadelphia: W.B. Saunders, 2002. P. 28192844.
7. Lee RK, AbolEnein H, Artibani W, Bochner B, Dalbagni G, Daneshmand S, et al. Urinary diversion after radical cystectomy for bladder cancer: options, patient selection, and outcomes. BJU Int 2014; 113(1):1123. doi: 10.1111/bju.12121
8. Stein JP, Skinner DG. Results with radical cystectomy for treating bladder cancer: a «reference standart» for highgrade, invasive bladder cancer. // BJU Int 2003; 92(l): 12